 Наявність в крові або сечі пацієнта онкомаркерів дозволяє при лабораторній діагностиці пухлин виявити наявність злоякісного новоутворення на ранніх стадіях. Для людей, які пройшли курс лікування від раку, існують рекомендації ВООЗ з приводу того, коли здавати аналізи на онкомаркери, також можуть бути призначені подібні дослідження і для тих, хто входить в групу ризику онкологічних захворювань. Так що ж визначають онкомаркери, і як їх використовують для здійснення моніторингу?
Наявність в крові або сечі пацієнта онкомаркерів дозволяє при лабораторній діагностиці пухлин виявити наявність злоякісного новоутворення на ранніх стадіях. Для людей, які пройшли курс лікування від раку, існують рекомендації ВООЗ з приводу того, коли здавати аналізи на онкомаркери, також можуть бути призначені подібні дослідження і для тих, хто входить в групу ризику онкологічних захворювань. Так що ж визначають онкомаркери, і як їх використовують для здійснення моніторингу?
Що таке онкомаркери, і що вони визначають
Завдяки використанню методів визначення пухлинних маркерів (онкомаркерів) набагато частіше, ніж через застосування загальноприйнятих методів діагностики виявляють рецидив та/або метастазування пухлини. У середньому це дозволяє зберегти час, що дорівнює 3-6 міс., а в окремих випадках — і більше року.
Протягом тривалого часу проводиться пошук лабораторних тестів ідентифікувати таких компонентів біологічних рідин, які б вказували на присутність в організмі пацієнта злоякісного процесу. Що ж таке онкомаркери і як їх використовують в діагностиці? Під онкомаркерами зазвичай розуміються речовини, що являють собою продукти зміненого метаболізму трансформованих клітин. Вони можуть бути визначені або за допомогою цитологічних методів дослідження (це так звані клітинні онкомаркери), або з використанням біохімічних методів аналізу сироватки крові або інших біологічних рідин.
В даний час під пухлинними маркерами (онкомаркерами) розуміються специфічні речовини різної хімічної природи), які є продуктами життєдіяльності злоякісних клітин або клітин, асоційованих зі злоякісним ростом, і виявляються в крові і/або сечі онкологічних пацієнтів. У більшості випадків це прості або модифіковані білкові молекули, що відносяться до глік – і липопротеинам. Деякі з них характерні тільки для однієї пухлини (тобто мають пухлинної специфічністю), інші зустрічаються при різних пухлинах.
Онкомаркери, що утворюються у самих пухлинних клітинах (пухлиноасоційовані онкомаркери), вивільняються з них у кров у ході розвитку онкологічного захворювання. Однак є і такі речовини, які, будучи асоційовані з пухлиною, зустрічаються також і в нормальних клітинах, тобто можуть у низьких концентраціях бути присутніми в організмі здорової людини. При цьому онкомаркери можуть знаходитися всередині або на поверхні клітини, їх частина секретується в кров, що дозволяє визначати їх методом імунологічного (імуноферментного, радиоиммунного) аналізу.
Далі ви дізнаєтеся, які бувають онкомаркери крові, і як їх використовують для моніторингу пухлинних захворювань.
Діагностика раку: які бувають види онкомаркерів крові
Всі типи онкомаркерів можна підрозділити на різні класи:
- асоційовані з пухлиною антигени або антитіла до них (визначаються методами імунологічного аналізу);
- продукти розпаду пухлин білкової природи;
- гормони (наприклад, хоріонічний гонадотропін людини, адренокортикотроцный гормон);
- ферменти (фосфатази, ізоферменти лактатдегідрогенази та ін); продукти азотистого обміну (креатин, гідроксипролін, поліаміни);
- нуклеїнові кислоти (вільна ДНК);
- специфічні білки плазми крові (феритин, церулоплазмин, бета-2-мікроглобуліну).
Відомі наступні види онкомаркерів для діагностики:
- раку яєчників,
- раку тіла і шийки матки,
- раку молочної залози,
- раку передміхурової залози,
- раку органів шлунково-кишкового тракту,
- раку легені,
- деяких інших злоякісних новоутворень.
Лабораторна діагностика пухлин: визначення біохімічних маркерів в крові
 Метод визначення онкомаркерів дозволяє не тільки діагностувати онкологічні захворювання на ранніх стадіях його формування, але і судити про ефективність і тактиці проведеного лікування, про прогнозі захворювання, тобто здійснювати моніторинг перебігу захворювання. Визначення виду онкомаркерів при діагностиці раку в динаміці онкологічного захворювання дає незрівнянно більшу інформацію, ніж його одиничне визначення. Встановлення рівня онкомаркерів в крові дуже важливо для прийняття рішення про припинення або продовження консервативної терапії.
Метод визначення онкомаркерів дозволяє не тільки діагностувати онкологічні захворювання на ранніх стадіях його формування, але і судити про ефективність і тактиці проведеного лікування, про прогнозі захворювання, тобто здійснювати моніторинг перебігу захворювання. Визначення виду онкомаркерів при діагностиці раку в динаміці онкологічного захворювання дає незрівнянно більшу інформацію, ніж його одиничне визначення. Встановлення рівня онкомаркерів в крові дуже важливо для прийняття рішення про припинення або продовження консервативної терапії.
Говорячи про те, які бувають онкомаркери, варто відзначити, що в даний час відомо більше 200 сполук, що належать до пухлинних маркерів, однак діагностичну значимість набуло визначення близько двадцяти біологічно важливих речовин (головним чином, білків і інших макромолекул).
Для остаточного підтвердження діагнозу методи дослідження онкомаркерів зазвичай поєднуються з проведенням інших діагностичних процедур.
Оскільки основні клінічні симптоми захворювання часом не проявляються на ранніх стадіях його формування, представляється особливо важливою рання діагностика онкологічної патології — насамперед з використанням лабораторних тестів на онкомаркери. До того ж нерідко навіть після виконання ранніх і радикальних операцій спостерігаються рецидиви і метастази пухлини. Їх виявлення сприяє визначення онкомаркерів при лабораторній діагностиці. Темп зростання рівня пухлинного маркера зазвичай дозволяє робити висновок про характер розвитку захворювання, зокрема про метастазуванні.
При регулярному спостереженні за показниками аналізів на онкомаркери, інформативних для конкретної локалізації пухлини, можна виявити метастази за 4-6 міс. до їх клінічного виявлення. Якщо після оперативного лікування або в процесі специфічної терапії не спостерігається зниження концентрації пухлинних маркерів, то це означає неефективність обраного способу лікування або проведеної операції (не радикально здійсненої).
Коли здають кров на онкомаркери: терміни аналізів
 Згідно з рекомендаціями ВООЗ, існують певні терміни, коли здають кров на онкомаркери. Частота взяття проб крові для визначення рівня онкологічних маркерів повинна становити:
Згідно з рекомендаціями ВООЗ, існують певні терміни, коли здають кров на онкомаркери. Частота взяття проб крові для визначення рівня онкологічних маркерів повинна становити:
- 1 раз на місяць протягом першого року після лікування;
- 1 раз в 2 місяці протягом другого року після лікування;
- 1 раз в 3 місяці протягом третього року спостереження;
- протягом наступних 3-5 років терміни аналізів на онкомаркери – двічі на рік або щорічно;
- після 6 років — щорічно.
Час виконання першої послеоперативной детекції концентрацій онкомаркера залежить від періоду його напівжиття в організмі. Як правило, першу послеоперативную детекцію онкомаркера виконують через 2-14 діб. після проведення операції. Графік визначень онкомаркера повинен відповідати клінічним станом конкретного пацієнта.
Підвищення концентрації онкомаркера в сироватці крові слід підтверджувати за допомогою повторної його детекції в наступній пробі крові, взятої дещо пізніше (тобто через 14-30 діб.). Вельми бажано підтвердити підвищення концентрацій у сироватці крові онкомаркера шляхом декількох повторних його визначень.
Наведені рекомендації, коли здавати аналізи на онкомаркери, є приблизними, оскільки час взяття проб крові для визначення біохімічних пухлинних маркерів при різних злоякісних новоутвореннях варіюється.
Графік визначення концентрацій онкомаркера повинен завжди відповідати клінічним станом конкретного пацієнта. У всіх випадках він повинен розроблятися на підставі аналізу динаміки зміни його концентрацій у плазмі (сироватці) крові.
Відхилення в рівнях одного або більше маркерів пухлинного росту відзначаються зазвичай у 80-90% пацієнтів, які страждають онкологічними захворюваннями.
На жаль, досі не представлений жоден пухлинний маркер, який володіє 100% діагностичною чутливістю і 100% діагностичною специфічністю по відношенню до якого-небудь одного органу.
Діагностичні показники аналізу крові на онкомаркери
 Діагностична надійність визначення пухлинних маркерів оцінюється рядом показників (діагностичної чутливості, діагностичної специфічності та ін).
Діагностична надійність визначення пухлинних маркерів оцінюється рядом показників (діагностичної чутливості, діагностичної специфічності та ін).
Такий показник аналізу крові на онкомаркери, як діагностична чутливість (ДЧ) лабораторного тесту, що характеризує відсоток позитивних результатів досліджень у онкологічних хворих. Наприклад, у випадку раку шлунка онкомаркер СА 12-4 характеризується діагностичною чутливістю 95%, це означає, що у 95 хворих на рак шлунка можна лабораторним шляхом встановити підвищений рівень онкомаркера, отже, у 5% пацієнтів з цією пухлиною рівень СА 72-4 не збільшується або не визначається.
Такий показник крові на онкомаркери, як діагностична специфічність (ДС), відображає відсоток виявлення негативного результату тесту у практично здорових людей (і/або хворих з іншими формами патології). Підвищення рівня онкомаркера може спостерігатися не тільки при злоякісному рості, але і при деяких інших патологічних і навіть фізіологічних процесах, і ДС відображає відсоток здорових індивідуумів, у яких результати детекції онкомаркера в плазмі крові є істинно негативними. ДС онкомаркера вказує на адекватність його використання в якості скринінгового параметра.
Ідеальною ситуацією є та, при якій величина діагностичної специфічності тесту дорівнює 100% (тобто відсутні хибнопозитивні результати даного тесту), що поєднується з максимально можливою величиною діагностичної чутливості (тобто детекцією щодо великої частини пацієнтів, що страждають онкологічними захворюваннями).
Прийнято вважати, що оптимальним варіантом для онкомаркера є 95% величина ДС при відповідній їй величиною ЧЧ. Якщо кілька онкомаркерів мають відносно даної пухлини приблизно однаковою ДЧ, кращим з них є той тест, який володіє найбільшою ДС.
Про діагностичної цінності онкомаркера представляється можливим судити на підставі характеру так званої ROC-кривої (ROC — receiver operating characteristics). Це діаграма, що відображає зв’язок між показниками діагностичної специфічності та діагностичної чутливості.
При аналізі концентрацій онкомаркерів в сироватці крові більш правильно говорити не про їх нормальних (референтних) величинах, а величини їх точок відсічення (cutoff) на рівні вищої межі ROC-кривої. Зазвичай в якості точки відсічення тіста використовують величину, відповідну 95 перцентилями нормальної популяції (здорових донорів).
В залежності від поставлених цілей величину встановленої точки відсічення можна змінювати. Наприклад, якщо ставиться завдання визначити найбільше число пацієнтів, що страждають злоякісним новоутворенням, точку відсічення онкомаркера знижують (підвищуючи тим самим ДЧ дослідження); однак це неминуче призведе до збільшення кількості хибнопозитивних результатів (тобто до зниження ДС дослідження).
З іншого боку, якщо ставиться завдання визначити істинність всіх отриманих позитивних результатів, слід збільшити значення точки відсічення тесту, таким чином, підвищуючи ДС дослідження, але разом з тим одночасно знижуючи його ЧЧ.
Внаслідок того, що підвищення концентрації ряду пухлинних маркерів може мати місце і при деяких доброякісних захворюваннях, для таких онкомаркерів часто визначають так званий діапазон концентрацій прикордонної («сірої» зони — інтервалу значень від верхньої межі норми (точки відсічення) до значення, характерного тільки для злоякісного новоутворення. Концентрація онкомаркера, що знаходиться в межах «сірої зони», вказує на необхідність виключення присутності в організмі пацієнта запального процесу або доброякісної пухлини.
У багатьох випадках величини концентрації онкомаркерів корелюють зі ступенем поширеності в організмі злоякісної пухлини або зі стадією її зростання.
Які повинні бути результати тестів на онкомаркери: допустимі показники
 Нижче описано, якими повинні бути результати «ідеальних» онкомаркерів.
Нижче описано, якими повинні бути результати «ідеальних» онкомаркерів.
Характеристика та використання тестів визначення онкомаркерів.
«Ідеальний онкомаркер» повинен:
- володіти здатністю 100% випадків диференціювати здорових індивідуумів від пацієнтів, які страждають злоякісними пухлинами;
- виявляти всіх онкологічних пацієнтів і по можливості — на самій ранній стадії розвитку злоякісної пухлини;
- володіти достатньою органної специфічністю, тобто такої, яка б дозволяла на підставі визначення концентрацій цього маркера в сироватці крові судити про точну органної локалізації злоякісної пухлини;
- володіти тісній прямій кореляційній залежності між величинами концентрації онкомаркера в сироватці крові та стадіями розвитку (зростання) злоякісної пухлини;
- відображати всі зміни, що відбуваються в пухлині, в процесі проведення онкологічного пацієнта протипухлинної терапії;
- володіти достатньо високою прогностичною значущістю.
Онкомаркер, що відповідає першим двом із перерахованих вимог, не може бути використаний для скринінгових цілей. Однак, оскільки серед відомих в даний час онкомаркерів таких не існує, жоден з ідентифікованих онкомаркерів не придатний для скринінгу нормальної, здорової популяції.
Оскільки «ідеального онкомаркера» поки не виявлено, застосування в клінічній практиці відомих допустимих показників онкомаркерів не рекомендовано для проведення загального скринінгу. Винятком з цього правила можна вважати простатспецифічний антиген, який в ряді країн використовується для скринінгу РПЗ у літніх чоловіків спільно з пальцевим ректальним дослідженням.
Принципи моніторингу онкомаркерів
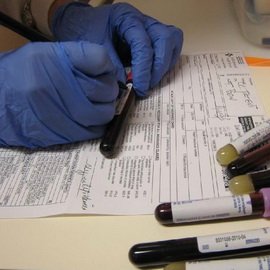 Визначення пухлинних маркерів в крові може використовуватися для здійснення моніторингу пацієнтів, які належать до груп високого ризику. До таких онкомаркерам, зокрема, відноситься АФП — для обстеження пацієнтів, носіїв HBsAg або страждають цирозом печінки, і кальцитонін — для пацієнтів із спадковою схильністю до С-клітинного (медуллярному) раку щитовидної залози. При відповідному застосуванні онкомаркерів для діагностики раку рецидив пухлини або її метастазів часто ідентифікують за місяці до їх клінічних проявів, що дозволяє ініціювати або коригувати пацієнтам проведення протипухлинної терапії в оптимальне для цього час.
Визначення пухлинних маркерів в крові може використовуватися для здійснення моніторингу пацієнтів, які належать до груп високого ризику. До таких онкомаркерам, зокрема, відноситься АФП — для обстеження пацієнтів, носіїв HBsAg або страждають цирозом печінки, і кальцитонін — для пацієнтів із спадковою схильністю до С-клітинного (медуллярному) раку щитовидної залози. При відповідному застосуванні онкомаркерів для діагностики раку рецидив пухлини або її метастазів часто ідентифікують за місяці до їх клінічних проявів, що дозволяє ініціювати або коригувати пацієнтам проведення протипухлинної терапії в оптимальне для цього час.
Встановлено, що на наступних стадіях пухлинного росту показники концентрації практично всіх онкомаркерів в сироватці крові мають більш високі значення, ніж на попередніх стадіях. Про можливості прогнозувати розвиток захворювання прийнято судити за показниками предсказательная цінності позитивного та негативного результатів тесту.
Як правило, онкомаркери не мають органоспецифичностью. Локалізація пухлини встановлюється методами імунної сцинтиграфії, що базується на застосуванні моноклональних антитіл.
Не всяка злоякісна пухлина локалізована в певному органі, экспрессирует один і той же пухлинний маркер. Для з’ясування того, які саме онкомаркери підходять для моніторингу протипухлинної терапії у конкретного пацієнта, доцільно перед проведенням йому хірургічної операції здійснити визначення не одного, а декількох онкомаркерів (так званої панелі онкомаркерів), що дозволяє вибрати той з них, показники концентрації якого будуть більш підвищені. Однак і ті онкомаркери, показники концентрації яких виявляються в межах норми, можуть згодом вказувати на можливість присутності в організмі пацієнта пізнього рецидиву пухлини або її метастазування.
Підвищені концентрації пухлинних маркерів у сироватці крові пацієнта можуть бути виявлені при ряді доброякісних захворювань. Зокрема, це відноситься до ряду речовин, в нормі містяться в тканинах печінки, це пов’язано з порушеннями процесів катаболізму і виведення речовини з організму (як правило, з жовчю). Зазвичай при цьому концентрації онкомаркерів знаходяться в межах низького патологічного діапазону (в «сірій зоні»). Таке підвищення концентрації онкомаркера в плазмі (сироватці) крові може бути передвісником печінкової недостатності або захворювань біліарного тракту.
В ранньому післяопераційному періоді або в процесі проведення пацієнту хіміо-або променевої терапії може відбуватися некроз тканини пухлини, що супроводжується короткочасним вивільненням з неї онкомаркерів в кров’яне русло. Така зміна концентрації онкомаркера не є індикатором збільшення її злоякісності.
Залежність результатів визначення змісту онкомаркерів від методології і технології дослідження
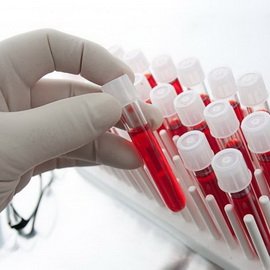 Показники концентрації онкомаркерів у сироватці крові пацієнта, встановлені за допомогою різних тест-систем, іноді можуть істотно відрізнятися. Ці відмінності обумовлені використанням антитіл, що взаємодіють з різними эпитопами одного і того ж антигену (наприклад, РЕА).
Показники концентрації онкомаркерів у сироватці крові пацієнта, встановлені за допомогою різних тест-систем, іноді можуть істотно відрізнятися. Ці відмінності обумовлені використанням антитіл, що взаємодіють з різними эпитопами одного і того ж антигену (наприклад, РЕА).
Відмінності в результатах дослідження можна очікувати і у випадку застосування в тест-системах однакових антитіл — внаслідок гетерогенної структури досліджуваного антигену, відповідних ефектів матриці та інших причин.
У разі якщо в клініко-діагностичної лабораторії починають застосовуватися тест-системи інших організацій-виробників, бажано виконати паралельне визначення концентрації онкомаркера в динаміці спостереження (в 2-3 пробах крові пацієнта).
Підвищені концентрації пухлинних маркерів у сироватці крові пацієнта також можуть бути наслідком інтерференцій, що виникають в процесі виконання тесту.
Вибір необхідних для виконання лабораторно-діагностичних досліджень °нкомаркеров визначається існуючими уявленнями про механізми виникнення і розвитку злоякісних пухлин, тобто про канцерогенезі.
Визначення пухлинних маркерів найбільш доцільно на тлі проведення пацієнту протипухлинної терапії (тобто хірургічна, хіміо-, променевої або гормональної терапії).
Базисний принцип моніторингу полягає в тому, що початкову концентрацію онкомаркера завжди визначають перед початком лікування.
У багатьох випадках величини концентрацій предоперативно детектованого онкомаркера корелюють з прогнозом, показниками загальної і безрецидивної виживаності пацієнтів. Тим не менш варто відзначити, що і «негативний» результат визначення не завжди виключає можливість присутності в організмі пацієнта злоякісної пухлини.
Якщо початкові показники маркерів онкологічних захворювань у сироватці крові пацієнта були підвищені, швидкий темп їх зниження вказує на те, що проведена цьому пацієнтові хірургічна операція була успішною, тоді як часткове зниження концентрації або повторне її підвищення вказують на те, що хірургічна операція здійснена успішно. Сталий повторне підвищення концентрації онкомаркера після проведених пацієнту курсів протипухлинної хіміотерапії може вказувати на необхідність її переривання або на внесення змін у тактику проведеної терапії.
Повторне підвищення в сироватці крові пацієнта концентрації онкомаркера через кілька місяців після вдало проведеної йому хірургічної операції часто є індикатором рецидиву пухлини або її метастазування. Причому таке підвищення концентрації онкомаркера може бути виявлено до клінічних проявів цих ускладнень.
Про рецидив або метастазуванні пухлини можна судити за характером динаміки збільшення концентрації онкомаркера і насамперед — по мірі її зростання. Так, незначне підвищення концентрації РЕА («низька» динаміка збільшення концентрацій онкомаркера) може вказувати на локальний рецидив пухлини або її метастазів у перитонеальну порожнину або в м’які тканини, в той час як «крута» динаміка зростання концентрацій цього онкомаркера (інтенсивна динаміка підвищення концентрацій онкомаркера) чітко вказує на процес метастазування пухлини в печінку та кістки.
Визначення онкомаркерів має величезне значення в моніторингу перебігу захворювання у онкологічних пацієнтів, що одержують протипухлинну лікування. У ситуації, коли злоякісні пухлини не відповідають на терапію, а у клініциста в розпорядженні є альтернативні варіанти її проведення, визначення відповідного, придатного для даного органу онкомаркера, часто в комбінації з іншим онкомаркером, може внести вирішальний вклад в успішне проведення протипухлинної терапії і тим самим значно підвищити ефективність лікування та поліпшити шанси пацієнта на виживання.
Далі ви дізнаєтеся, які аналізи здають на онкомаркери, і як це робиться правильно.
Які аналізи роблять на онкомаркери і як їх правильно здавати
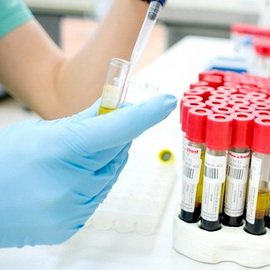 Визначення концентрації онкомаркерів може проводитися в сироватці (плазмі) крові, сечі, цереброспінальної, насіннєвий, амніотичній та інших біологічних рідинах організму.
Визначення концентрації онкомаркерів може проводитися в сироватці (плазмі) крові, сечі, цереброспінальної, насіннєвий, амніотичній та інших біологічних рідинах організму.
Щоб здати аналіз крові на онкомаркери, напередодні не можна вживати алкоголь, медикаменти, курити. Аналіз виконується натще.
Для отримання сироватки венозну кров, узяту, як правило, з ліктьової вени, слід відразу після взяття помістити у воду з льодом і негайно доставити в лабораторію.
Сироватка крові стабільна при 2-8°С протягом 24 год і більш тривалий період часу — при заморожуванні до температури 20°С (або нижчу). Слід уникати повторних циклів заморожування-розморожування.
Для деяких тестів необхідно ввести в отриману сироватку антикоагулянт. В якості останнього зазвичай використовуються ЕДТА (этилендиаминтетраацетат) або гепарин.
А як правильно здавати аналіз сечі на онкомаркери? Для отримання придатної для дослідження сечі слід звільнити сечовий міхур (ранкова сеча для аналізу непридатна), випити 200 мл води, зібрати годинну порцію сечі, помістити у воду з льодом і негайно доставити в лабораторію; в разі виконання відстрочених досліджень пробу сечі заморозити і доставити в лабораторію. Встановлюють pH сечі близько 6,0 (зазвичай внесенням в неї гідроксиду натрію). Далі пробу сечі слід отцентрифугировать і довести рн до 7,0. Проба сечі (свіжий зразок) повинна бути використана для дослідження протягом 2-3 год (на аналіз зазвичай потрібно 10 мл сечі).
Мало здати аналізи на онкомаркери – зразки цереброспінальної рідини слід перед дослідженням отцентрифугировать. Зразок стабільний при -20°С до 6 міс., при -70°С — невизначено довго. Переважно використовувати зразки цереброспінальної рідини без липемии або гемолізу.